Нарушение формирования пола
Формирование пола проходит целый ряд последовательных этапов: формирование гонад, формирование внутренних гениталий, формирование наружных гениталий и, наконец, формирование вторичных половых признаков. Регулирование этого процесса осуществляется генетическими и гормональными факторами.
Эмбриогенез
Между 4 и 5 неделями развития плода происходит формирование первичных гонад. Кариотип здорового человека состоит из 44 аутосом и 2 половых хромосом. На генном уровне пол эмбриона определяется набором половых хромосом X и Y. Несмотря на то, что Y хромосома содержит лишь около 2 % гаплоидного генома, она содержит гены, контролирующие формирование пола. При оплодотворении яйцеклетки формируется генетический пол будущего ребенка. При оплодотворении яйцеклетки сперматозоидом, несущим Х-хромосому, генетический пол будущего ребенка женский (набор половых хромосом ХХ), при оплодотворении яйцеклетки, сперматозоидом, несущим Y-хромосому, генетический пол будущего ребенка мужской (набор половых хромосом XY). В настоящее время определена локализация около 100 генов в Y хромосоме. Основными из них являются: SRY (sex determining region Y chromosome), DAX-1 (dosage-sensitive Sex-reversal), TDF (testis determining factor), ZFY, TSPY (testis specific protein), AZF (фактор азооспермии), HY-ген фактора гистосовместимости, GBY ген [Черных В.Б. и соавторы, 2001; Lopez M. et al 1995; Cantrell M.A. et al, 1998]. Для образования мужской половой гонады необходимо присутствие Y хромосомы. Установлено, что на Y-хромосоме расположен ген, ответственный за синтез специфического поверхностного белка – HY антигена. Именно этот антиген и определяет развитие половой закладки в мужскую гонаду.
Итак, при наборе половых хромосом, содержащем Y-хромосому, формируется яичко, но полноценное яичко формируется лишь при наличии Х и Y-хромосом. Для правильного формирования яичка необходимо присутствие не менее двух Х-хромосом. Полноценная женская гонада формируется при кариотипе 46ХХ.
В дальнейшем идет развитие как внутренних, так и наружных гениталий. На ранних этапах развития эмбриона отмечается наличие женских (мюллеровы) и мужских (вольфовы) протоков. Закладкой внутренних половых органов являются 2 пары протоков: мюллеровы и вольфовы, открывающиеся в урогенитальном синусе. Из мюллеровых протоков образуются женские внутренние половые органы из вольфовых соответственно мужские. Формирование внутренних и наружных гениталий у плода мужского пола – активный процесс. Клетки Сертоли в эмбриональных тестикулах начинают активно синтезировать фактор, подавляющий у плода мужского пола развитие мюллеровых протоков. Клетки Лейдига в яичках все значительнее секретируют тестостерон под влиянием, которого вольфовы протоки дифференцируются в семенные пузырьки, семявыносящий протоки и придаток тестикула. При отсутствии активного воздействия фактора, ингибирующего Мюллеровы протоки, происходит развитие мюллеровых протоков, дифференцирующихся в дальнейшем в матку, верхней части влагалища и фаллопиевые трубы. Вольфовы же протоки при этом регрессируют. Наружные гениталии и уретра у плодов обоего пола развиваются из общей закладки - урогенитального синуса и полового бугорка, генитальных складок и возвышений.
Формирование внутренних половых органов
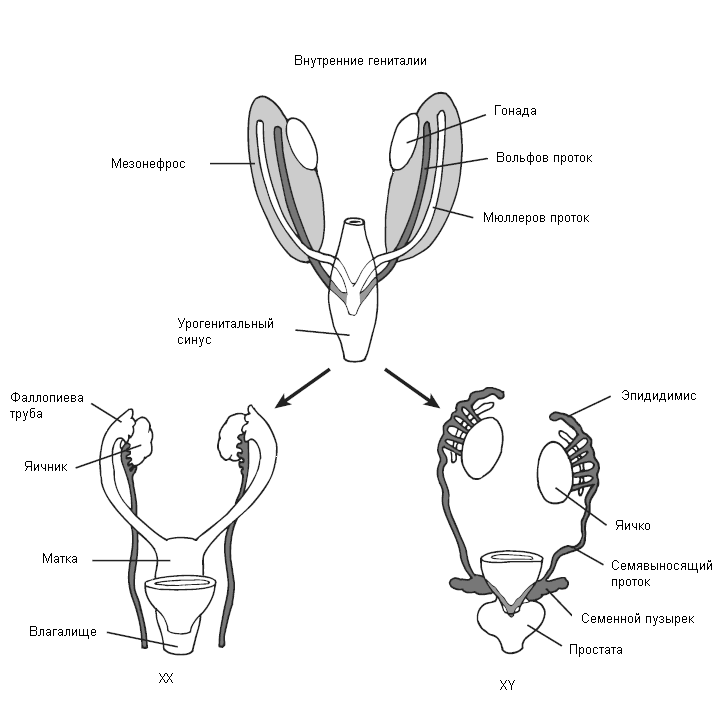
Начиная с 10-й недели внутриутробного развития, фетальный тестикул сначала под влиянием хорионического гонадотропина (ХГ), затем собственного лютеинизирующего (ЛГ) гормона синтезируют большое количество тестостерона, влияющего на образование наружных гениталий. Помимо тестостерона для дифференцировки наружных половых органов необходимо так же воздействие активного метаболита тестостерона – дигидротестостерона, который образуется непосредственно в тканях под влиянием фермента 5-альфа-редуктазы. Под влиянием гормонов урогенитальный синус преобразуется в простату и внутреннюю часть уретры. Уретральные складки и валики трансформируются в пениальную уретру и пещеристые тела полового члена. Генитальный бугорок формирует головку полового члена. Меатус головки формируется путем втяжения эпителиальной ткани, которая соединяется затем с уретральной бороздой в области ладьевидной ямки. В конце первого триместра происходит окончательное формирование гениталий.
Формирование наружных гениталий
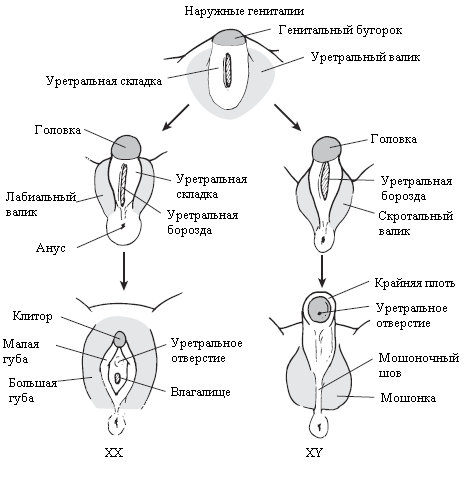
Таким образом, к моменту рождения половой аппарат ребенка полностью сформирован. У здоровых детей пол гонад, строение внутренних и наружных органов, т.е. фенотип или морфологический пол полностью соответствует кариотипу, т.е. генетическому полу.
В постнатальном периоде жизни ребенку предстоит пройти еще очень важный этап полового формирования - пубертатный период, период полового созревания. Следовательно, лишь к концу пубертатного периода полностью заканчивается формирование полового аппарата здорового человека. С этого времени человек способен к выполнению основной биологической функции - к воспроизведению себе подобных.
1. Патология формирования пола
Основная причина патологии полового формирования – хромосомные или более тонкие генетические аномалии. При этом может иметь место нарушение числа или структуры половых хромосом, или непосредственное повреждение генов, ответственных за половое формирование. Половое формирование может нарушаться и при патологии аутосом или, вернее, генов, локализующихся на аутосомах, но принимающих непосредственное участие в половом формировании. Значительно реже пороки развития полового аппарата у ребенка могут быть обусловлены нарушением гормонального баланса беременной женщины (прием гормональных препаратов, гормонально активные опухоли) и (или) гормональной функции плаценты.
Воздействие вышеперечисленных неблагоприятных патологических факторов, нарушающих нормальные процессы формирования пола, может идти двумя путями:
- Патологические факторы препятствуют формированию полноценной гонады, что в свою очередь нарушает процессы формирования гениталий.
- Формирование гонады не нарушается. В этих случаях патология полового аппарата может быть обусловлена врожденным дефектом синтеза тестостерона или метаболизма дигидротестостерона, нарушением чувствительности тканей мишеней к действию половых гормонов, повышением уровня половых гормонов внегонадного происхождения.
1.1 Агенезия гонад
Воздействие неблагоприятных факторов на ранних этапах эмбриогенеза может воспрепятствовать формированию гонады. Наиболее часто агенезия гонад является результатом патологии (нарушение числа или структуры) половых хромосом, реже у подобных больных находят нормальный для женщин или мужчин набор половых хромосом (чистая агенезия гонад).
При любой причине, вызвавшей состояние гонадального агенеза, клиническая картина заболевания во многом будет одинаковой. На месте гонад, там, где обычно располагаются яичники, у этих больных находятся образования, которые представляют собой белесоватые полоски соединительной ткани – «streak». Подобная «гонада» формируется раньше, чем начинается дифференцирование половой закладки в яичко или яичник. Само собой разумеется, то подобная «гонада», не содержащая фактически функциональных элементов половой железы, не способна выделять половые гормоны ни в период внутриутробной жизни, ни в последующие годы. Этим и объясняется наличие женского фенотипа и выраженных симптомов гипогонадизма у всех больных с гонадальным агенезом. В данном случае, в результате отсутствия функционирующей гонады, формирование внутренних и наружных гениталий обусловлено автономной тенденцией плода к феминизации. У всех больных находят атрофичную матку с трубами, узкое влагалище. Наружные гениталии всегда женского типа, лишь малые половые губы могут быть недоразвитыми. При рождении таких детей никогда не возникают сомнения в принадлежности ребенка к женскому полу. В детском возрасте у таких «девочек» очевидных симптомов заболевания, свидетельствующих о патологии полового формирования, нет. Патология полового аппарата проявится значительно позже, когда будет обращать на себя внимание отсутствие вторичных половых признаков. Симптомы гипогонадизма у таких больных резко выражены: молочные железы не развиваются, менструации не приходят, полового оволосения нет. (Касаткина Э.П., 1979, Grumbach M.M., 1989).
1.2 Дисгенезия гонад
Подобная патология возникает на более поздних этапах эмбриогенеза, в тот момент, когда из половой закладки начинает формироваться мужская или женская гонада. Однако воздействие неблагоприятных факторов препятствует окончательному формированию полноценной половой железы.
При дисгенезии гонад, в отличие от агенезии, клинические проявления при повреждении мужской или женской гонады буду различными.
1.2.1 Дисгенезия яичников
Наиболее частой причиной дисгенезии яичников является мозаичный кариотип 45Х0/46ХХ. Клеточный клон с нормальным для женщины набором половых хромосом обеспечивает дифференцирование половой закладки в яичник. Наличие патологического клеточного клона мешает окончательному формированию полноценной гонады. Степень недоразвития гонады зависит от процентного соотношения нормальных и патологических клеточных клонов и распределения их в организме. При преобладании патологического клеточного клона половая железа будет напоминать соединительнотканную полоску при гонадальном агенезе, но с более выраженными клеточными элементами коркового слоя. При преобладании нормального клеточного клона гонада может представлять собой гипопластичный яичник.
У части больных с этой патологией выявляют нормальный женский кариотип 46ХХ.
Итак, при дисгенезии яичников фенотип больных всегда бывает правильный женский. Следовательно, в детском возрасте очевидных симптомов патологии полового формирования нет. Лишь впоследствии, на фоне пубертатного периода выявляется гипогонадизм.
1.2.1 Дисгенезия яичек
В отличие от ранее описанных нарушений полового формирования дисгенезия яичек клинически характеризуется смешанным строением гениталий.
Причиной внутриутробного повреждения (недоразвития) яичка у части больных с дисгенезией гонад является нарушение числа половых хромосом. При некоторых клинических вариантах заболевания выявляется или предполагается по клиническим проявлениям мозаицизм типа 45Х0/46ХY. В редких случаях обнаруживают выраженные структурные изменения половых хромосом. У части больных причину внутриутробного повреждения яичка выявить не удается: набор половых хромосом у этих больных нормальный для здоровых мужчин. Однако наличие при некоторых клинических вариантах заболевания семейного характера позволяет предположить генетическую патологию. При значительной степени повреждения яичка гонада при дисгенезии тестикулов может представлять собой мало дифференцированную ткань, внешне напоминающую «streak», но с несколько большим содержанием тестикулярной ткани. У части больных гонада более дифференцирована и визуально представляет собой гипоплазированное яичко с морфологическими признаками внутриутробного повреждения.
Фенотип таких больных практически всегда ближе к женскому, внутренние гениталии всегда женского типа. Женское строение внутренних гениталий (наличие матки, труб и верхней части влагалища) у этих больных обусловлено недоразвитием клеток Сертоли и дефицитом антимюллерова вещества. Отсутствие семявыносящего протока и женское строение наружных гениталий у этих больных обусловлено дефицитом тестостерона в период внутриутробной жизни. Небольшие количества тестостерона, которые синтезируют эти «гонады» способны лишь сформировать вирилизованный клитор (резко недоразвитый половой член), т.к. половой бугорок в период внутриутробной жизни наиболее чувствителен к действию андрогенов. В постнатальный период жизни такие яички оказываются абсолютно несостоятельными, т.е. имеет место выраженный гипогонадизм и бесплодие. Подобный характер повреждения гонад наблюдается при следующих клинических вариантах заболевания: синдроме Шерешевского-Тернера с гермафродитными гениталиями, чистой дисгенезии яичек, синдроме рудиментарных яичек.
Редким вариантом внутриутробной патологии яичек является такое состояние, когда повреждается лишь морфогенетическая функция эмбриональных тестикул. При этом чаще имеет место дефицит лишь антимюллерова вещества. Половой аппарат мальчика, а именно половые протоки и наружные гениталии, формируются у таких больных по мужскому типу, но при этом имеет место хорошо развитая матка и трубы. Обычно подобный порок развития выявляется случайно (во время оперативного вмешательства). Вторичные половые признаки у таких больных всегда хорошо развиты (тестостероновая функция не нарушена), часть больных фертильна. Клиническим вариантом подобной патологии является синдром Рейера.
1.3 Внутриутробная атрофия яичек
У плода с нормальным мужским кариотипом на разных стадиях внутриутробного развития происходит атрофия яичек. В зависимости от сроков повреждения яичек формируются разные варианты патологии пола. Так, при повреждении яичек на ранних этапах (до 12 недель) внутриутробной жизни формируется клиника гермафродитизма. При повреждении яичек вскоре после 12 недель – микрофалус. В остальном гениталии (внутренние и наружные) сформированы правильно по мужскому типу. Атрофия гонад в более поздние сроки развития плода не оказывает влияние на дифференцировку пола: гениталии формируются по мужскому типу, половой член нормальных размеров. При всех вариантах внутриутробной атрофии яичек на фоне пубертатного периода имеет место выраженный гипогонадизм.
Обычно при дисгенезии яичек гонады с обеих сторон недоразвиты в одинаковой степени. Однако довольно часто наблюдается ассиметричное развитие гонад. При этом с одной стороны имеется дисгенетический семенник, с другой – рудиментарная гонада или вторая гонада вообще отсутствует – смешанная дисгенезия яичек. У больных с ассиметричным расположением гонад довольно часто наблюдается ассиметричное развитие внутренних гениталий. При наличии матки со стороны рудиментарной гонады имеется труба, а со стороны семенника может быть развит только семявыносящий проток или мужские и женские протоки одновременно.
1.4 Формирование смешанной гонады
У части больных патология формирования пола проявляется в том, что обе зоны половой закладки развиваются в гонады, т.е. из половой закладки одновременно формируются элементы и мужской и женской гонады. Чаще выявляют правильный женский кариотип (46ХХ) или значительно реже – правильный мужской (46ХY). Иногда имеет место мозаичный кариотип.
1.5 Внутриутробный дефицит тестостерона
У части больных с нормальным мужским кариотипом (46ХY) и мужскими гонадами патология формирования пола может быть обусловлена дефицитом тестостерона в период внутриутробной жизни. Дефицит тестостерона может быть обусловлен врожденным дефектом стероидогенеза тестостерона или врожденным дефицитом гонадотропных гормонов (ГТГ).
Дефект синтеза тестостерона у большинства больных является результатом дефицита одной из пяти ферментных систем, участвующих в синтезе гормона в надпочечниках и гонадах. Гонады таких больных, как правило, нормально развиты и не имеют морфологических признаков повреждения. Состояние генетически обусловлено, тип наследования – аутосомно-рецессивный.
Дефицит тестостерона, который имеет место у больных с подобными дефектами, в период внутриутробной жизни является причиной формирования смешанных гениталий и гипогонадизма. У большинства больных фенотип приближается к женскому: половой член недоразвит, мошонка расщеплена, имеется слепозаканчивающееся влагалище, которое открывается в гипоспадированную уретру. На фоне пубертата вторичные половые признаки не формируются.
Значительно реже (при частичном дефиците ферментов) фенотип больных приближается к мужскому. На фоне пубертата у таких больных может быть спонтанное развитие вторичных половых признаков мужского типа. Обращает на себя внимание, что у большинства больных с врожденным дефектом синтеза тестостерона на фоне пубертата формируется гинекомастия неясной этиологии.
Внутриутробный дефицит тестостерона, помимо нарушения его синтеза, может быть обусловлен врожденным дефицитом лютеинизирующего гормона (ЛГ) или нарушениями чувствительности гонад к действию ЛГ. Секреция тестостерона клетками Лейдига фетальных яичек на ранних этапах внутриутробной жизни (первые три месяца) регулируется хорионическим гонадотропином, на более поздних этапах – ЛГ плода. Поэтому врожденный дефицит ЛГ или нарушение чувствительности гонад к действию ЛГ могут быть причиной дефицита тестостерона на более поздних этапах внутриутробной жизни, когда дифференцировка пола закончена и формируются кавернозные тела, увеличивается в размерах половой член. Данное патологическое состояние характеризуется наличием микрофалуса, в остальном наружные гениталии сформированы по мужскому типу. Впоследствии у больного выявляются симптомы гипогонадизма. Внутренние гениталии сформированы по мужскому типу.
Таким образом, врожденный дефицит тестостерона способствует формированию клиники ложного мужского гермафродитизма или микрофалуса.
1.6 Нарушение действия тестостерона на уровне тканей
Данное патологическое состояние характеризуется нормальным функционированием яичек, достаточным уровнем тестостерона в период внутриутробной жизни и в последующие годы.
Однако тестостерона на уровне андрогензависимых тканей не оказывает маскулинизирующий эффект. Это может быть обусловлено двумя причинами: нарушением чувствительности рецепторов андрогензависимых тканей к тестостерону и дефицитом фермента 5α-редуктазы, превращающего тестостерон в его активную форму – дигидротестостерон.
При наличии любой из этих причин отсутствие эффекта тестостерона на уровне тканей в период внутриутробной жизни препятствует формированию мужского фенотипа.
Нарушение чувствительности к андрогенам является причиной достаточно распространенного варианта ложного мужского гермафродитизма – синдрома тестикулярной феминизации.
При полной потере чувствительности к андрогенам формируется женский фенотип. На фоне пубертатного период формируются вторичные половые признаки женского типа. Развитие вторичных половых признаков женского типа можно объяснить тем, что у подобных больных на уровне тканей снимается конкурирующее действие андрогенов и при этих условиях небольшие количества эстрогенов могут оказать хороший феминизирующий эффект.
При частичной потере чувствительности к андрогенам формируются смешанные гениталии. На фоне пубертатного периода у таких больных наблюдается в разной степени выраженная андрогенизация.
Следует отметить, что при любом строении наружных гениталий внутренние гениталии у больных сформированы по мужскому типу.
Нарушение чувствительности к андрогенам – генетически обусловленное состоянии. Наблюдается большой процент семейных случаев. Заболевания всегда передают женщины, носительницы патологического гена, а болеют только мужчины.
Дефицит 5α-редуктазы также является причиной формирования смешанных гениталий. В результате дефицита активной формы тестостерона (ДГТ) наружные гениталии плода формируются под влиянием автономной тенденции к феминизации. Фенотип таких больных ближе к женскому. Однако на фоне пубертата нередко имеет место спонтанное развитие вторичных половых признаков.
1.7 Высокий уровень тестостерона в перид внутриутробной жизни внегонадного происхождения.
Подобные патологические состояния являются причиной формирования распространенной формы гермафродитизма – ложного женского гермафродитизма.
Наиболее частый вариант ложного женского гермафродитизма – врожденная дисфункция коры надпочечников. Врожденная дисфункция коры надпочечников обусловлена патологией аутосом, заведующих ферментативным синтезом стероидных гормонов коры надпочечников. Заболевание имеет рецессивный тип наследования. При этом заболевании имеет место дефицит ферментных систем, принимающих участие в синтезе глюко- и менералокортикоидов. В результате нарушения синтеза жизненноважных гормонов резко повышается уровень АКТГ. В ответ на это надпочечники гиперплазируются и выделяются в избытке те стероиды, в синтезе которых дефектные ферментные системы участия не принимают, т.е. андрогены. Таким образом, клиническая симптоматика этого заболевания обусловлена дефицитом жизненноважных гормонов и избыточным содержанием андрогенов. У плода женского пола избыточное содержание андрогенов, способствует вирилизации наружных гениталий. При этом формируются наружные гениталии полностью мужского типа или смешанные гениталии.
Высокий уровень андрогенов в период внутриутробной жизни может быть результатом приема матерью мужских половых гормонов или результатом наличия у нее андрогенпродуцирующих опухолей яичников или надпочечников.
1.8 Прием матерью во время беременности прогестиновых препаратов и эстрогенов.
Прием подобных препаратов во время беременности может вызвать вирилизацию женского пола или феминизацию мужского пола.
Таким образом, у генетического мужского плода смешанное строение гениталий может быть результатом формирования неполноценного яичка, нарушения гормональной функции эмбриональных яичек или нарушения чувствительности к действию андрогенов. При этом происходит формирования смешанных гениталий.
У плода женского пола смешанное строение гениталий обусловлено избыточным содержанием андрогенов в период внутриутробной жизни, чаще надпочечникового происхождения. У части больных формируется смешанная гонада и как результат – смешанное строение гениталий.
Классификация гермафродитизма:
- Ложный мужской гермафродитизм
Дисгенезия яичек: синдром Шерешевского-Тернера, чистая дисгенезия яичек, синдром рудиментарных яичек.
Врожденные дефекты биосинтеза тестостерона: дефицит десмолазы, дефицит 3β-ОН-дегидрогеназы, дефицит 17α-гидроксилазы, дефицит 17,20-лиазы, дефицит 17β-ОН-дегидрогеназы.
Дефицит 5α-редуктазы
Синдром тестикулярной феминизации: синдром полной тестикулярной феминизации, синдром неполной тестикулярной феминизации.
- Ложный женский гермафродитизм
Врожденная дисфукция коры надпочечников
Ненадпочечниковые формы
- Истинный гермафродитизм
Классификация микрофалуса: синдром внутриутробной атрофии яичек, врожденные нарушения гонадотропной регуляции (врожденный дефицит Г.Т.Г., нарушение чувствительности к ЛГ)
Автор статьиХирург андролог-уролог КМН Демин Н. В.Выпускник Российского национального исследовательского медицинского университета имени Н.И. Пирогова (бывший РГМУ)
Кандидат медицинских наук. Тема диссертационной работы: «Лечение свищей уретры с использованием методов тканевой инженерии».
С 2015 года доцент кафедры эндоскопической урологии ФПК МР РУДН.Член Европейского общества детских урологов (ESPU)
Член Европейской Ассоциации урологов (EAU)
Член профессиональной Ассоциации андрологов России (ПААР)



